데이터완전성 (Data Integrity) = ALCOA+ 또는 ALCOA++ 로 이해하고 계신 분이 많은데, ALCOA+ 가 Data Integrity 와 동의어로 사용되는 것은 아니며 정확히 하면 ALCOA+ 로 표현되는 요구 기준 항목들(ALCOA CCEA)이 데이터 수명주기(생애주기, Lifecycle) 전반에서 반영되어야 함을 간단히 설명하기 위한 목적으로 만들어진 약어입니다. (ALCOA 기원 참조)
ALCOA 에서 ALCOA + (CCEA) 로 강화되고, 최근에는 ALCOA++ (ALCOA CCEA T, Traceable/Traceability 추가) 개념까지 강화되고 있습니다. 본 포스팅에서는 Data Integrity를 이해하는 데 중요한 개념인 “ALCOA++”에 대해 정리합니다.
ALCOA++ 란?
ALCOA++ 는 데이터의 완전성(=완결설=무결성) 준수를 통해 의약품 품질을 보장하기 위한 중요 GMP 개념 중 하나로, 제약산업에서 특히 준수 되어야 하는 중요한 사안입니다. 본래 ALCOA+ 로 활용되었으나, 최근 ‘Traceability’에 개념이 추가되었습니다.
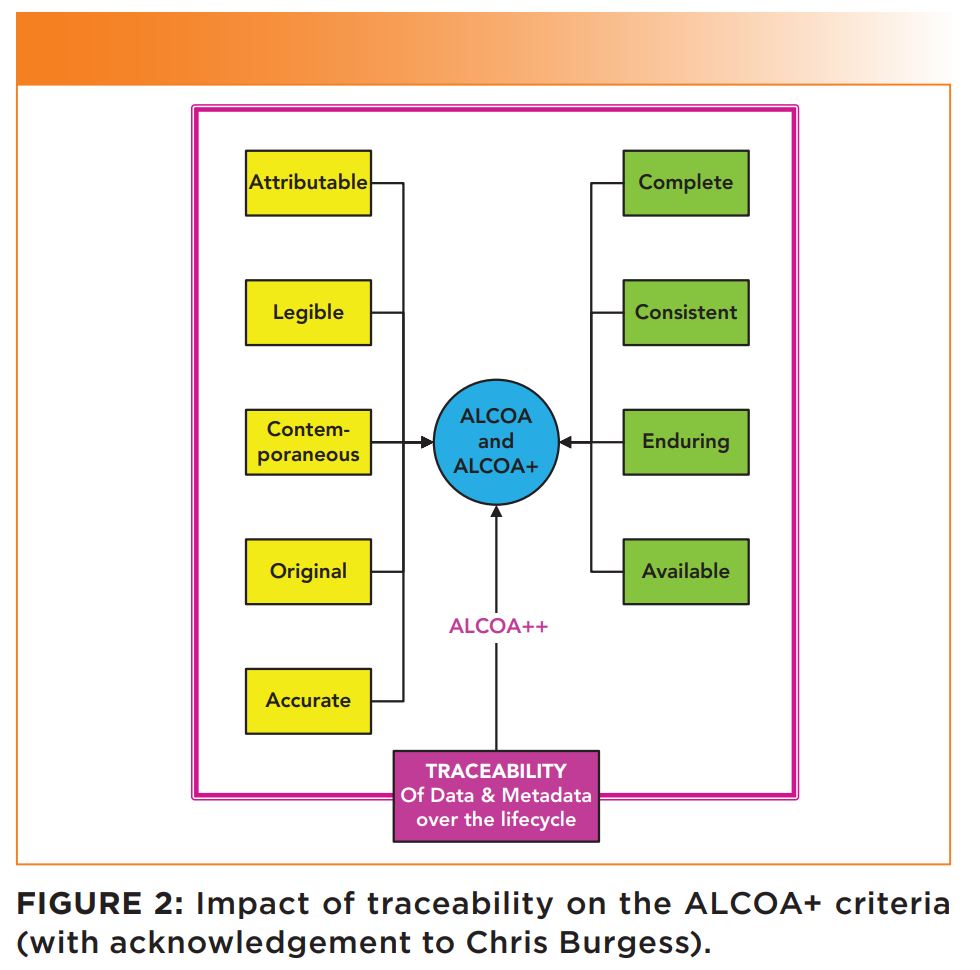
ALCOA++는 “Attributable, Legible, Contemporaneous, Original, Accurate, Complete, Consistent, Enduring, Available, and Available + Traceability” 의 약어입니다. 2021년 EMA (European Medicines Agency) 의 a guidance on electronic source data in clinical trials 에 처음 정의가 포함되었습니다.
ALCOA++ 는 GMP 환경에서 생성된 모든 데이터의 무결성을 보장하기 위한 핵심 원칙 사항이며, 기존 ALCOA+ 와 ㅆTraceable/Traceability 가 추가된 ALOCA++ 의 관계에 대한 이해가 필요합니다. 넓은 범주에서는 기존 9 개 항목(ALCOA+) 에 하나의 기준이 추가된 10개 ALCOA+ 로 이해하는 것도 가능하지만, Traceable 요소는 기존 9개 항목 자체 범주를 넘어서는 전체 범주에서의 DI 완결성을 위한 개념으로 이해할 수 있습니다. 이 요구 기준들은 GMP 데이터가 신뢰할 수 있음을 설명할 수 있으며 특히, 허가 규제 기관(규제 당국) 에서 요구하는 생산 제조 및 품질 데이터의 완결성 준수를 위한 핵심 요구 기준입니다. (데이터의 생성, 가공, 변경, 보고, 보관, 유지 및 폐기 등의 과정에서)
기존 ALCOA+ 에서는 각 핵심 요구 기준의 반영과 정책/절차 준수를 위한 가이드를 제공했으며, 추가된 ‘Traceability’는 데이터의 ‘추적성’ 을 의미하나, 더 넓은 범주에서는 기존 ALCOA+ 요소 간의 결합 및 개별 요소들에 대한 추적성을 부여하고 관리, 평가를 통해 데이터 완전성 범주에서의 요구 기준 준수를 더욱 강화 시키는 목적에 있습니다.
예를 들어, 데이터의 귀속성 (누가, 언제, 무엇을 만들고, 변경하고, 처리했는지 등의 귀속 정보의 부여) 자체가 기본 DI 요구 기준 사항으로 적용되어야 하지만, 이러한 귀속성 또한 기존 데이터의 귀속 정보 자체의 변경(업데이트)에 따른 구/신 정보가 생성되는 전 과정에서의 추적성(Traceability) 이 반영되어야 함을 의미합니다.
ALCOA++ 중요성
ALCOA++ 는 의약품의 품질과 GMP 규정, 규제를 준수하는 데 필수 요소입니다. 그 이유는 GMP 업무 전반 (생산/제조/포장, 물류(원료/자재 관리), 품질 시험, 시설 운영, 허가, 출하 및 불만 관리 등) 에서 일어나는 활동(작업, 평가, 보고, 승인 등)에 대해서 그것을 증명할 수 있는 서명, 기록, 자료가 요구되기 때문입니다.
서명, 기록, 데이터(자료) 의 신뢰는 GMP 활동(=작업, 모든 절차) 의 신뢰 기준이 되므로, 서명/기록/데이터의 조작 및 위변조는 GMP 활동의 신뢰를 깨는 것이며 이는 의약품의 품질 또한 보증할 수 없음 (제조 및 품질 시험의 적합성을 신뢰할 수 없음)으로 평가됩니다.
따라서, ALCOA++ 요구 기준에 따라 수립된 적합한 정책(거버넌스 포함)과 절차를 통해 DI 요구기준이 준수된 환경에서 생성된 서명/기록/데이터는 제품의 안전성과 효과성을 보장할 수 있으며, 규제 기관과 협력하며 제품의 품질을 입증하는 데 중요한 역할을 합니다. 특히, ALCOA CCEA 요소들과 함께 전 항목 기준 영역에서 상호관계에서도 Traceability 를 갖춤으로써 데이터 생성 부터 폐기 까지의 전 수명주기 동안의 History 를 추적할 수 있고, 이를 통해 데이터 완정성 오류나 부정확성을 식별하여 데이터의 신뢰성을 더욱 강화할 수 있습니다.
ALCOA++ 요소
프로세스 ALCOA++ 원칙을 준수하기 위한 프로세스는 다음과 같습니다.
▼ ALCOA 요소
Attributable (귀속성):
데이터는 원본(Original record)의 출처와 연결되어야 합니다. 즉, 생성된/가공된 데이터는 누가, 언제, 어떻게 데이터를 생성/가공했는지 귀속 정보를 확인할 수 있어야 합니다.
Legible (가독성):
데이터는 명확하게 기록되어야 하며, 데이터와 연관된 모든 작업자/관계자가 읽고 이해할 수 있어야 합니다.
Contemporaneous (동시성):
데이터는 사건(작업/절차 등)이 발생한 동안 실시간으로 기록되어야 하며, 시간이 역전되거나 사후에 임의로 시간을 역전해 수정되어서는 안 됩니다.
Original (원본성):
데이터는 원본(Original) 형태로 유지되어야 하며, 절차나 시스템 검증 없이 임의로 복사한 사본은 원본의 효력을 인정할 수 없습니다. 원본 데이터는 임의 변경이나 조작이 없어야 합니다.
Accurate (정확성):
데이터는 실제 기록, 절차, 작업 상황을 정확하게 반영(계산, 기록) 해야 하며, 오류가 없어야 합니다.
▼ plus (+) 요소
(2010년 추가 – EMA, a guidance on electronic source data in clinical trials)
Complete (완전성):
데이터는 필요한 모든 정보 (Raw data + meta data) 를 포함해야 하며, 누락되거나 생략되어서는 안 됩니다.
Consistent (일관성):
데이터는 일관된 형식과 표준을 따라야 하며, 다른 데이터와 일관성이 유지되어야 합니다.
Enduring (영속성):
데이터는 필요한 기간 동안 안전하게 보관되어야 하며, 무결성과 안정성을 유지해야 합니다.
Available (가용성):
데이터는 필요한 이해 관계자에게 언제든지 접근 가능해야 하며, 검토와 감독에 사용될 수 있어야 합니다.
▼ plus/plus (++) 요소
(2021 추가- EMA, Guideline on computerised systems and electronic data in clinical trials)
Traceable / Traceability (추적성):
데이터는 데이터 수명 주기(생애주기) 동안 추적 가능해야 합니다. Audit trail 의 목적과 기능으로 이해하시면 이해가 좀 더 쉽습니다. 데이터에 발생한 모든 변경 사항들은 정확하게 추적할 수 있고, 문서화 되어야 합니다.

Traceability의 역할
Traceability는 데이터의 변경(수정) 이력을 추적함으로써 데이터의 신뢰성을 확보할 수 있는데, 데이터 수정 시 왜 수정되었는지, 누가 수정했는지, 언제 수정되었는지 등의 Meta data 정보(=귀속정보)를 제공함으로써 데이터 신뢰를 높이고 데이터의 변경 이력을 식별하는 데 도움을 줍니다.
Traceablility 는 귀속정보 단위(범주)의 추적 능력을 뛰어 넘어 사건의 인과관계 및 시간의 흐름관계, 작업의 프로세스 과정에서의 추적성을 포함합니다. 예를들어 분석 시험에 사용된 장비/기기/소모품/glassware 등이 어떻게 세척, 운영, 관리 되고, 어떤 절차로 평가되는지 등의 절차(적합기준/관리기준을 포함)의 추적을 가능하게 하여 특정 STEP 이전/이후 단계를 포괄하는 데이터 완전성 준수를 보장하도록 합니다.
ALCOA++ 준수를 위해 필요한 것
적합한 Data Integrity 거버넌스 수립
GMP 전 영역에서의 데이터에 대한 관리와 운영, 평가를 위한 전반적인 DI 거버넌스가 수립되어야 하고, 이에 따라 데이터의 중요도 및 흐름, 위험 요소의 정의 및 관리에 대한 정책이 ALCOA++ 요구 기준 하에 동반되어야 합니다.
지속적인 Data Integrity 교육
DI 준수를 위한 적절한 Quality Culture 를 조성하기 위해서는 일시적인 교육 보다는 지속적인 (단계적인) 교육이 요구됩니다. 특히, 생산/제조, QC 등의 독립된 조직 내에서의 관행, 관습에 부딪히는 DI 요구기준에 대해서 단계적 적응이나 현실적인 Supporting 이 필요합니다.
기술적 지식:
데이터 완전성 요구기준 (ALCOA++) 은 절차를 통해 반영, 적용될 수 있으나, 많은 부분에서 컴퓨터화 시스템을 포함한 장비/설비/기기의 적절한 설정 수준 또는 Application S/W 에 대한 이해를 요구합니다. 따라서, 생산/제조, QC 부서 등의 실무 부서에서 역량이 도움이 되며, 실제 DI 문제 사항을 경험하고 이를 이해하는 것이 DI 정책/절차 개선에 도움이 됩니다.
더 많은 포스팅 읽기